热线:021-66110810,66110819
手机:13564362870


热线:021-66110810,66110819
手机:13564362870
摘要:中国盐碱地形成,大部分与土壤中碳酸盐的累计有关,因而碱化度普遍较高。在盐碱地再利用过程中,简单说,可以分为轻盐碱地、中度盐碱地和重盐碱地。利用NaCl、Na2SO4、NaHCO3、Na2CO34种盐,按不同比例配比,人工模拟盐碱地中轻盐碱地盐碱度、中度盐碱地盐碱度和重盐碱地盐碱度。
选用耐盐苜蓿品种金皇后、中度耐盐苜蓿品种阿尔冈金、敏感苜蓿品种敖汉,分别进行盐碱胁迫实验;通过非损伤微测技术检测苜蓿根系Na+、K+离子流变化,比较轻盐碱度、中度盐碱度和重盐碱度胁迫下3个耐盐苜蓿品种的离子流速差异。结果显示:在盐碱胁迫下,耐盐碱品种金皇后Na+离子流速外流速度比中度耐盐品种阿尔冈金要高,且均表现为外流;敏感品种敖汉在中度盐碱环境下由外流转变为内流,并出现萎蔫迹象。3个苜蓿品种的K+离子流速都发生变化,表现为外流,但流速变化各不相同且无明显的规律性。所以,在盐碱抗逆性中紫花苜蓿可以通过Na+离子流速控制来适应盐碱环境。
干旱、盐碱等非生物逆境胁迫时常严重影响植物的正常生长发育,也是导致农作物减产的重要环境因素。植物在长期的进化过程中,在分子、细胞和生理生化水平上均已形成应对外界不良环境的一系列应答机制。紫花苜蓿(MedicagosativaL.cv)是世界上分布最广泛的豆科牧草,也是中国种植面积最大的饲草饲料作物,在发展畜牧业生产、改良土壤和保护生态环境等方面发挥着重要的经济、生态和社会效益。目前土壤盐碱化已成为制约中国农业发展的重要问题,并影响到生态系统的稳定和生物的多样性。紫花苜蓿作为一种非常重要的豆科牧草,培育抗盐、抗碱的苜蓿新品种具有重要的现实迫切性。
本实验利用NaCl、Na2SO4、NaHCO3、Na2CO34种盐,按不同比例配比,人工模拟盐碱地中轻盐碱地盐碱度、中度盐碱地盐碱度和重盐碱地盐碱度,选用耐盐苜蓿品种金皇后、中度耐盐苜蓿品种阿尔冈金、敏感苜蓿品种敖汉分别进行盐碱胁迫实验;通过非损伤微测技术检测苜蓿根系Na+、K+离子流速变化,比较轻盐碱度、中度盐碱度和重盐碱度胁迫下耐盐苜蓿品种的差异,该研究可为紫花苜蓿耐盐碱育种研究提供新的理论支持。
1材料与方法
1.1材料
耐盐型紫花苜蓿品种:金皇后(God Empress);中度耐盐型紫花苜蓿品种:阿尔冈金(Algonquin);盐敏感型紫花苜蓿品种:敖汉(Aohan)。
1.2材料培养
1.2.1苜蓿种子萌发
种子用3%的次氯酸钠溶液消毒15 min,75%的酒精清洗2~3次。蒸馏水浸种20~24 h后,挑选萌发一致的种子置于培养皿中,培养皿中铺垫单层滤纸,用蒸馏水浸湿滤纸,每天置换滤纸,培养3~5 d后移植。
1.2.2盐碱混合胁迫处理
盐碱地利用的简单分类:轻度盐碱地pH值为7.1~8.5,中度盐碱地pH值为8.5~9.5,重度盐碱地pH值为9.5以上。实验中用A1组、A2组、A3组分别表示轻度盐碱地(A1组:V(NaCl):V(Na2SO4):V(NaHCO3):V(Na2CO3)=1:2:1:0,pH值7.77±0.104)、中度盐碱地(A2组:V(NaCl):V(Na2SO4):V(NaHCO3):V(Na2CO3)=1:9:9:1,pH值8.80±0.043)、重度盐碱地(A3组:V(NaCl):V(Na2SO4):V(NaHCO3):V(Na2CO3)=1:1:1:1,pH值9.84±0.013)。人工模拟盐碱地盐碱浓度混合比见表1。
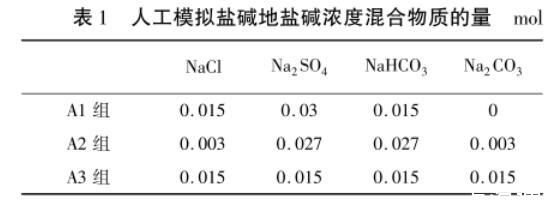
表1人工模拟盐碱地盐碱浓度混合物质的量mol
将萌发一致的紫花苜蓿幼苗移栽花盆,每盆5苗,3次重复,先用蒸馏水浇灌,一次浇透,每隔2 d浇一次。缓苗30 d后,用不同盐碱混合溶液进行混合胁迫,每盆80 mL盐碱混合液,分4次浇灌,每次间隔2 d。每隔24 h用PHS-3C型数字pH计测定流出液的电导率、pH值,连续测定至pH值基本不变为止(盆下流出液体的pH值、盐分浓度与实验设计的要一致)。对照组不处理。处理共计10 d。盐碱胁迫浓度设置空白组A0(正常盐碱度)、A1组(轻度盐碱度)、A2组(中度盐碱度)、A3组(重度盐碱度)。
1.3方法
1.3.1Na+离子流速检测
Na+离子流速检测利用非损伤微测系统(YoungerUSA(Xuyue Beijing)NMT Service Center)完成。以非损伤性扫描离子选择电极技术获取进出紫花苜蓿根系的Na+离子浓度(mmol·L-1级)、流速及流向信息。离子选择性电极由玻璃微电极、Ag/AgCl导线、电解质及液态离子交换剂(LIX)组成。该电极在待测离子浓度梯度中以已知距dx进行两点测量,可测得两点的电压分别为V1、V2,再通过已知的该电极的电压/浓度校正曲线计算离子的浓度。通过物理学中的离子/分子扩散定律的数学公式:J0=-D*dc/dx,可获得该离子的流动速率(pmol·cm-2·s-1)。式中,D为离子/分子特异的扩散常数(cm-2·s-1)。本实验所用微电极均为旭月公司提供。Na+选择性微电极前端灌充250 Lm Na+离子的液态交换剂液柱,后端灌充有15~50 mm左右的电解液柱(100 mmol·L-1NaCl),将电极固定器上的Ag/AgCl丝从电极后面插入,使其与电解液接触。固体电极作为参比电极。玻璃微电极需要校正后使用,校正斜率在58±3范围内为合格电极,可用于检测。校正液中Na+的浓度分别设置为0.1和1 mmol·L-1,其他成分与测试液相同。
幼苗在测量前10 min转移到装有测试液(0.1mmol CaCl2,0.1mmol KCl,0.5 mmol NaCl,0.2 mmol Na2SO4,0.3 mmol MES,pH值5.8)的测试盒中平衡。测试时,将幼苗根系置于测试液中,用小玻璃块将测试部位固定压好。测量区域是位于距离根尖300~400 um的根系根毛区。将电极尖端置于距离根表10 Lm处作为原点,在垂直于根表面的方向进行两点移动,测量两点电压差,两点移动距离为30 Lm(如图1)。每个样品稳定测量10 min。
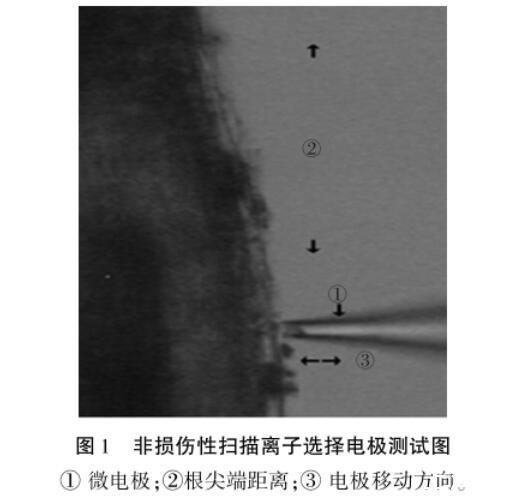
图1非损伤性扫描离子选择电极测试图①微电极;②根尖端距离;③电极移动方向。
所测结果利用校正得到的Nernst slope将测量两点之间电压差换算成离子浓度差。再将结果代入Fickcs第一扩散定律,就可获得该离子的流动速率(pmol·cm-2·s-1)。在试验中,流速计算利用Mage flux软件(YoungerUSA Sc.i&Tech.Corp.,USA)完成。在净离子流的计算过程中,基本上认为根表面离子流运动符合圆柱扩散几何模型。
1.3.2K+离子流速检测
K+离子流速的测定方法与Na+离子流速的测定方法相同。
 相关新闻
相关新闻