热线:021-66110810,66110819
手机:13564362870


热线:021-66110810,66110819
手机:13564362870
研究简介:本论文研究了中间神经元在癫痫样放电(epileptiform discharges,EDs)期间对血流动力学和代谢反应的贡献。研究通过在麻醉大鼠的感觉皮层中同时记录局部场电位(LFPs)、单个神经元放电、血流和氧水平,揭示了中间神经元活动在神经血管耦合中的重要作用。癫痫是一种常见的神经系统疾病,其发病机制与大脑皮层神经元的异常放电密切相关。癫痫发作期间,神经元的过度兴奋会导致局部脑血流和代谢的变化,这种变化可以通过功能性磁共振成像(fMRI)等技术进行检测。然而,目前对于神经元活动与血流动力学反应之间的耦合机制尚不完全清楚,尤其是在兴奋性和抑制性神经元对血流动力学信号的贡献方面。本研究旨在通过多模态记录技术,深入探讨中间神经元在癫痫样放电期间的血流动力学和代谢反应中的作用。研究使用了11只雄性Wistar Han大鼠作为实验对象。通过在感觉皮层注射bicuculline(一种GABAA受体拮抗剂)诱导癫痫样放电。实验中同时记录了多单位活动(MUA)、局部场电位(LFPs)、脑血流(CBF)和组织氧分压(PO2)。通过一般线性模型(GLM)分析神经参数(如单单位和多单位活动)对血流和代谢反应的预测能力。
Unisense微电极系统的应用
Unisense微电极被用于测量组织氧分压(PO2)。使用的是Clark式氧气微电极,其尖端直径为10微米,微电极连接到一个PA2000主机(unisense).采用两点校准法,将电极插入33°C的生理盐水溶液中,分别在95%氧气或环境空气中平衡,以校准电极。微电极被放置在与bicuculline注射点相近的位置,用于测量局部组织氧分压的变化.。PO2信号与LFP、CBF信号同时被记录,采样频率为1250 Hz。微电极的尖端直径仅为10微米,能够实现对局部脑组织氧分压的高精度测量,从而准确反映癫痫样放电期间组织氧水平的动态变化。
实验结果
研究结果表明,在癫痫样放电(EDs)期间,中间神经元(INT)活动以及放电幅度和频率是神经血管耦合的重要因素。需要进一步的计算研究来测试包含这一变量的模型行为,从而更好地解释BOLD fMRI信号与神经元活动之间的关系。一个关键问题是研究癫痫EEG-fMRI研究中的负性BOLD响应,但整个领域都将受益于更完善的模型。最终可以设计模型来估计隐藏参数(即模型中存在但无法直接测量的参数),并改进癫痫患者致痫神经组织的无创术前定位。因此,fMRI可以单独使用或与同步EEG记录结合使用,以替代神经外科植入的颅内立体脑电图电极或表面阵列的筛查(这些方法不仅存在风险,而且需要长时间住院)。中间神经元活动在癫痫样放电期间的血管和代谢反应中起着重要作用。中间神经元的活动比主细胞的活动更能预测血流和氧反应,这可能与中间神经元在神经血管耦合中的直接作用有关。这些发现对于解释fMRI研究中观察到的血流动力学变化具有重要意义,尤其是在癫痫研究中。
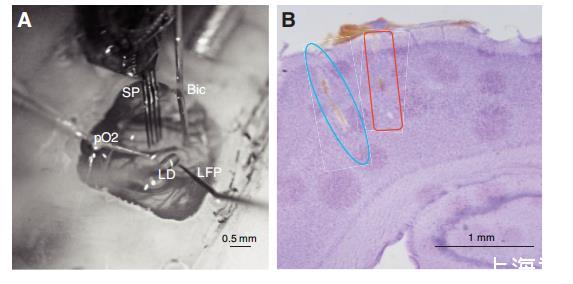
图1、A:展示大鼠癫痫样放电(EDs)模型活体同步记录实验设置的颅骨开窗照片。该模型通过体感皮层注射荷包牡丹碱(Bic)诱导,实验装置包括:用于多单元电活动(MUA)记录的硅探针(SP)、记录局部场电位(LFP)的钨电极、监测脑血流量(CBF)的激光多普勒探头(LD)以及检测组织氧分压(PO2)的氧探头。B:尼氏染色脑切片显示记录区域,标注注射位点(蓝色椭圆)及硅探针单侧电极排的植入位置(红色方框)。
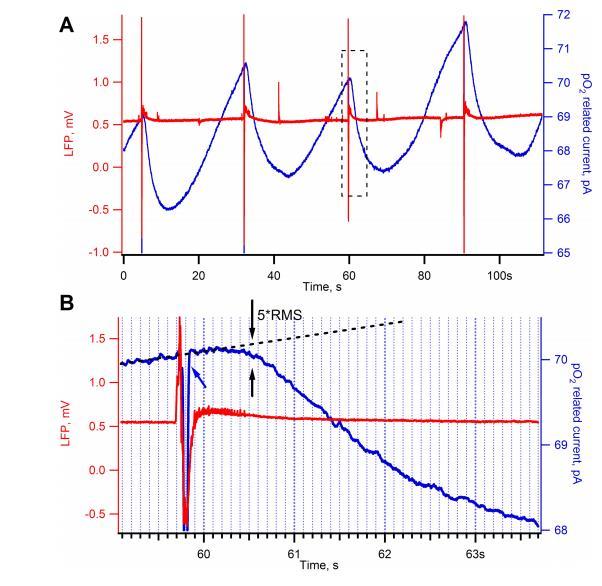
图2、氧分压(PO2)探头延迟时间的评估。采用离体完整海马组织,通过荷包牡丹碱诱导癫痫样放电(EDs)。A:7日龄小鼠海马组织在10μM荷包牡丹碱诱导EDs(红色曲线)期间的氧相关电流信号(蓝色曲线)。B:为评估每次ED与氧消耗起始之间的时间延迟,从氧信号中减去基线斜率(黑色虚线)。消耗起始点定义为:经基线校正后的氧相关电流振幅达到基线噪声均方根(RMS)振幅5倍时的时刻(黑色箭头)。
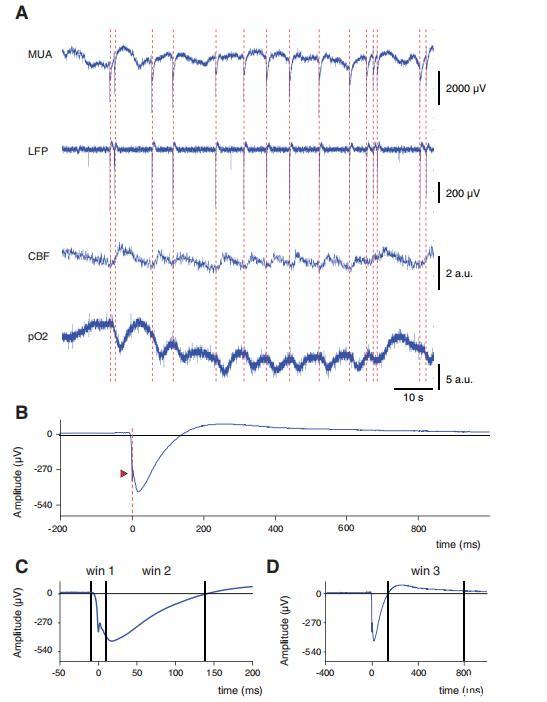
图3、对癫痫样放电(EDs)的多模态响应。A:同步多模态记录数据,包括硅探针采集的多单元电活动(MUA)、场电极采集的局部场电位(LFP)、激光多普勒测量的脑血流量(CBF)以及氧探头测量的组织氧分压(PO2)。红色虚线标记每次放电的起始时间点(time 0)。a.u.表示任意单位。B:A图中单个ED的放大显示。红色箭头指示用于设定time 0的极尖锐峰值。C:分别对应锐波上升支(win1)和下降支(win2)的时间窗放大图。D:对应EDs慢波成分(win3)的时间窗放大图。
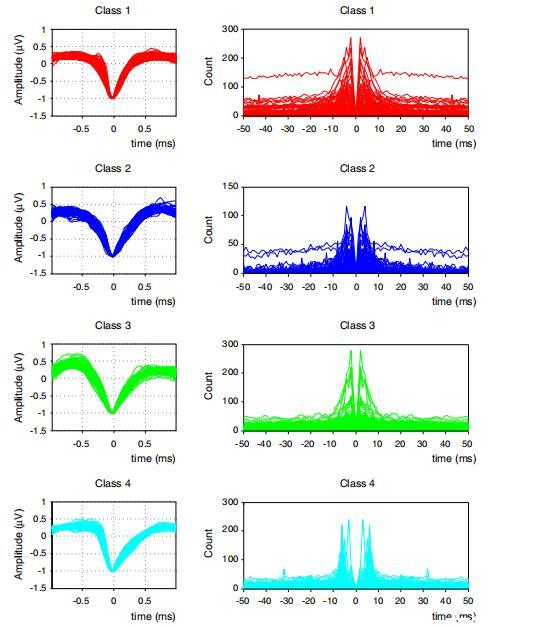
图4、神经元分类为假定主细胞(PCs)与中间神经元(INTs)。左图:基于主成分分析的四类神经元波形图。右图:对应的自相关直方图(ACG)。

图5、血流动力学与代谢响应函数(HRF)。A:通过反卷积计算获得的各只大鼠CBF脉冲响应函数。B:基于大鼠1的CBF响应(黑色),拟合的gamma函数HRF1(红色)和HRF2(蓝色)。C:所有大鼠经反卷积获得的PO2响应。D:大鼠1的PO2响应拟合gamma函数。需注意大鼠间存在显著变异(体现在响应幅值及后半段形态差异:CBF表现为向基线的漂移,PO2则出现超调)。ED发生时刻定义为时间0。
结论与展望
在癫痫中血流动力学反应的解释受到对神经血管耦合机制理解不足的限制,尤其是兴奋和抑制的贡献。研究人员在麻醉大鼠的体感皮层同步进行了多模态记录,包括局部场电位(LFPs)、单个神经元放电、血流和氧水平。通过注射荷包牡丹碱诱导的癫痫样放电被用于触发强烈的局部事件。局部场电位与血流存在强耦合关系,局部场电位与组织氧水平亦是如此。研究人员对402个神经元的记录分析显示,血流/组织氧与假定的中间神经元放电相关,但与主要细胞无关。结果表明中间神经元活动在癫痫样放电期间的血管和代谢反应中具有重要作用。unisense微电极的尖端直径仅为10微米,能够实现对局部脑组织氧分压的高精度测量,从而准确反映癫痫样放电期间组织氧水平的动态变化,为研究神经血管耦合提供了重要的代谢指标,在参数化线性模型中,局部场电位以及脑血流和组织氧分压的基线活动对血流和氧反应有显著贡献。研究结果表明,中间神经元(INTs)的活动与血流和氧反应之间的相关性高于主细胞(PCs),这一发现是基于Unisense微电极所记录的氧分压数据得出的,从而为理解神经血管耦合的细胞机制提供了重要线索。本研究不仅增进了对癫痫发作期间神经血管耦合机制的理解,还为未来的研究提供了新的方向,例如开发更准确的模型来解释fMRI信号与神经活动之间的关系,以及改进癫痫患者术前癫痫灶定位的方法。