热线:021-66110810,66110819
手机:13564362870


热线:021-66110810,66110819
手机:13564362870
砷(As)是一种象牙色的类金属,能在270℃时转变为金属样形式,被广泛应用于医学、畜牧养殖、电子和冶金等领域。早在2003年,中国地方性砷中毒分布调查协作组发现,中国受砷中毒影响人口达234万,高砷暴露人口52万;此外,智利的3个州有43万人受到砷污染的危害;石臼湖中砷的浓度超过了江苏省的土壤重金属背景值。近年来,砷污染已成为全球性问题,砷被国际癌症研究机构认定为致癌物质。环境中的砷以三价砷(As(Ⅲ))、五价砷(As(Ⅴ))和有机砷的形态存在,以As(Ⅲ)和As(Ⅴ)为主。砷形态极易受氧化还原条件、pH值、Fe(Ⅱ)/Fe(Ⅲ)、有机物、悬浮颗粒和微生物活动等环境因素的影响。形态不同的As所产生的生态效应也不同,As(Ⅲ)的毒性是As(V)的60倍,是甲基砷的70倍。As(Ⅲ)和As(Ⅴ)易被地表广泛存在的铁、锰化合物吸附聚集,污染土壤和沉积物,目前我国沿海区域沉积物中As的平均质量分数已接近10 mg/kg。As(Ⅲ)比较活跃,沉积物间隙水中的As(Ⅲ)可释放进入上覆水中,而进入水环境的As污染物可通过食物链最终影响人体健康。
沉积物-水界面中的As去除效果取决于复杂的物理、化学和生物作用,影响因素众多,作用机制复杂,一直是重金属内源污染研究和治理的难点。砷污染是可治理的,如淮河干流中的砷就得到了控制。目前砷去除方法有生物炭吸附、离子交换、植物修复、膜技术和沉淀絮凝等。生物炭/铁酸锰能对Zn2+和Cu2+两种重金属离子起到较好的吸附效果,铁锰可能在砷的吸附上也会有较好的效果。崔晓倩等发现莱茵衣藻能够影响自由金属离子的溶出;刘爱荣等指出,纳米零价铁可以有效去除废水中的砷。砷还可以通过植物光合作用和呼吸作用调节次级代谢产物,五价砷酸盐与磷酸盐有相似的化学性质,能共用高等植物中的转运蛋白被植物一同吸收,有些耐砷植物可通过改变转运蛋白的表达来控制砷的吸收。陈同斌等率先在中国境内找到并发现了蜈蚣草对砷的高富集性;Kumar等证实了胭脂树叶生物吸附剂能够去除水中的As;陈国粱通过培养试验对比研究了苦草、狐尾藻、黑藻、菹草、金鱼藻等沉水植物对沉积物砷的富集能力,发现苦草的富集能力最强。一般而言,水生植物对水环境中重金属去除效果的顺序为:沉水植物大于漂浮植物、浮叶植物大于挺水植物。可见,植物的同化吸收作用可以从土壤和沉积物中移除As。研究植物对沉积物中砷的去除对人体健康和生态安全具有重要意义。本文以富营养化底泥和常见沉水植物苦草为研究对象,基于微电极分析技术和高分辨率扩散平衡式间隙水采集(HR-Peeper)技术,从微尺度精准评估苦草对沉积物-水界面中As形态的影响。
1材料与方法
1.1研究区域概况
本文所用水样和沉积物样品均采集于太湖梅梁湾。梅梁湾位于太湖北部区域,面积约123km2,多年平均水深介于1.8~2.3 m之间。近年梅梁湾长期存在水体富营养化及与富营养化相关的问题。
1.2室内试验设计与试验材料
底泥样品用重力取样器(直径9cm、长50cm)采集在同一地点柱芯深度25cm左右的柱状样。湖水用5L采水器采集,并暂存于25L塑料桶中。样品采集完成后尽快运至实验室。随后,将沉积柱每2cm切割,并将相同的沉积层放在一起搅拌混匀。然后,使用100目的筛网从沉积物中去除大颗粒和大型底栖动物。根据原深度回填规则混匀过筛后的底泥,将8层(约16cm)的底泥装入6根有机玻璃管(内径9cm、长度30cm)。向每个沉积柱中注入过滤后的湖水,确保上覆水的深度在10cm左右。最后,将所有沉积柱放入水箱中(长70cm、宽50cm、高65cm)培养2周。
过滤后的湖水水质指标如下:湖水As质量浓度为1.22μg/L,TOC、TN、TP、磷酸根分别为7.43mg/L,0.93mg/L,0.04mg/L,0.02mg/L,pH值为7.57。用离心法得到过筛混匀后分层底泥的间隙水,测定间隙水中溶解态As、As(Ⅲ)和As(Ⅴ)的质量浓度(表1)。
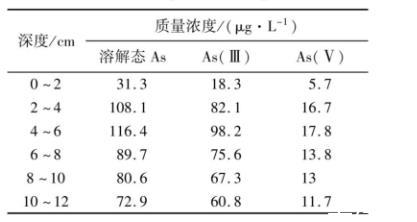
表1过筛混匀后的间隙水中溶解态As、As(Ⅲ)和As(Ⅴ)质量浓度
稳定两周后,取出沉积柱,在其中3根沉积柱中种植苦草,作为苦草组,苦草的种植密度为157.2株/m2;剩余3根不处理,作为对照组。分别将苦草组和对照组置于2个水箱中淹没培养,并用LED灯补充光照,在前15d对两个水箱进行曝气,以确保苦草的成活率,15d后取消曝气。
1.3样品采取和分析
对苦草的生长初期,快速生长期以及稳定生长期内沉积物变化进行观察,分别在第15天、第35天、第66天进行取样观测。在每个采样时间点,先用ph微电极(OXO-50,Unisense,丹麦)测量苦草组和对照组沉积物-水界面中的pH值和DO浓度。然后,投入HP-Peeper装置(购自南京智感环境科技有限公司),平衡时间为48 h。移除HR-Peeper装置后,从每个HR-Peeper小室收集大约400 uL的水样,用邻菲咯啉比色法在多功能酶标仪(M2e,Molecular Devices,美国)上测定可溶性Fe(Ⅱ)。取一定量样品添加3%HNO3酸化后,用ICP-MS(NEXION350 X,PerkinElmer,美国)测量溶解态As和溶解态Mn的质量浓度。本试验中所用的化学试剂均为分析纯。
1.4数据分析
采用SPSS 25.0软件(US SPSS)和Excel 2013进行统计分析,图形均用Origin 2019软件绘制。
 相关新闻
相关新闻