热线:021-66110810,66110819
手机:13564362870


热线:021-66110810,66110819
手机:13564362870
用于刺激视网膜神经元的电子视网膜假体有望恢复视力。然而,传统视网膜植入物的刚性电极会对软视网膜组织造成损害。由于它们与退行性视网膜中的靶细胞的接近程度较差,因此它们的选择性也有限。
近日,延世大学材料科学与工程系的Jang-Ung Park教授,眼科的Suk Ho Byeon教授以及釜山国立大学有机材料科学与工程系的Seung Geol Lee教授报道了一种柔性人造视网膜,具有直接打印的3D LM微电极,能够进行微创视网膜刺激。体内实验表明,可见光照明诱导了光线入射的局部视网膜区域的RGCs的尖峰活动,表明活rd1小鼠具有视力恢复的潜力。这些结果对不均匀视网膜变性患者的个性化人工视网膜的开发具有预后意义。其主要研究方向为以电化学为基础的柔性可穿戴仿生器件的制备及应用。
相关工作以“Liquid-metal-based three-dimensional microelectrode arrays integrated with implantable ultrathin retinal prosthesis for vision restoration”为题发表在Nature Nanotechnology上。
基本内容
视网膜变形疾病通常会造成感光细胞逐渐丧失或者永久性损伤,从而导致严重的视力损害。然而,视网膜内层神经元能够得以保留,该组织的电激活能够产生视觉感知(光幻视),这使得制备利用光响应装置电刺激内层视网膜神经元的电子视网膜假体成为一种有前景的恢复视力的方法。值得注意的是,人类受试者及相关手术表明视网膜和植入物之间的不一致(例如电极与细胞之间的距离,细胞与设备之间的机械适配)是限制该设备成效和应用的主要原因。为了解决这一限制,人们研究了超薄柔性光电器件以将其共形地附着在弯曲的视网膜表面上,但扁平形状的电极会导致局部凹凸不平的视网膜表面产生几何间隙。三维(3D)微电极有望有效刺激神经系统,缩短电极与细胞之间的距离。此外,它们可以通过绕过不应被刺激的神经元来刺激选择性局部区域,从而提供出色的选择性和高空间分辨率。但是,先前报道的3D神经电极往往利用刚性固态材料,这可能或直接损害柔软的视网膜或导致视网膜内的炎症反应。
为了应对这些挑战,该研究团队公布了一种软人造视网膜,将柔性、超薄和光敏晶体管阵列与液态金属(LMs)的软3D刺激电极集成在一起,用于视力恢复。其中,低毒性软共晶镓铟合金(EGaln)液态金属被3D打印为具有高分辨率的刺激电极,相对于以前使用的刚性柱状/尖峰电极材料相比,最大限度地减少了视网膜的不良损伤。此外,局部涂覆在这些EGaln-LM电极尖端上的铂(Pt)纳米团簇能够有效地将电荷注入视网膜神经元。机器学习应用于动物实验期间产生的输出信号,以分析诱发的视网膜神经节(RGC)棘波。并在体内实验证实了可见光照射引起的信号放大在光入射局部区域的视网膜神经节细胞中引起实时反应,能够使患有大量感光细胞变性的活视网膜变性(rd1)小鼠恢复视力,有望应用于治疗人类视网膜变性相关疾病并促进视力修复。
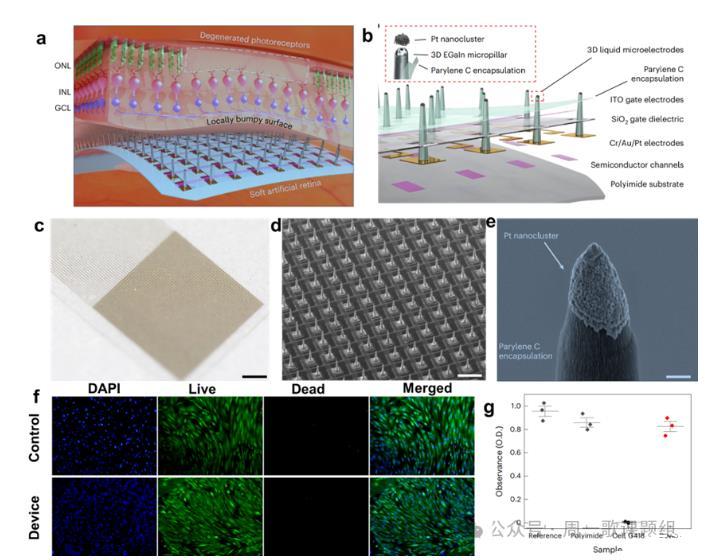
图1.采用3D LM微电极阵列的软人工视网膜。
首先,作者介绍了3DLM微电极阵列软人工视网膜的结构和体内外生物相容性。该微电极(图1a)能够紧邻不均匀变性视网膜表面,LMs突出的柔软柱状探针直接刺激视网膜神经节细胞(RGCs)。从该器件结构的布局来看(图1b),EGaln微柱阵列通过3D打印直接印刷在光电晶体管的漏电极表面上,柱子侧壁被聚对二甲苯C层封装,顶端电镀了铂纳米团簇(铂黑PtB)增加了微电极的纳米级粗糙度和它们的电化学表面积。光电晶体管用于产生光电流,增大漏极电流,并在漏极电压的脉冲刺激下,通过微电极注入RGCs的电荷显著增加,然后在RGCs内诱发的动作电位传递到视神经,从而替代视觉信息。这种人造视网膜结构将高分辨率晶体管阵列和3D LM微电极集成在一起,每个微电极尖端均具有PtB涂层,且这些涂层没有改变EGlan本身的弹性模量(图1c-1e)。为了确保该装置的体内/体外生物相容性,作者使用人视网膜色素上皮细胞的活/死细胞进行了细胞生存能力的测试以及在植入活体rd1小鼠五周后相关免疫和神经毒性的测试,结果表明该装置满足医疗器械的体外/体内毒性标准(图1f-1g)。
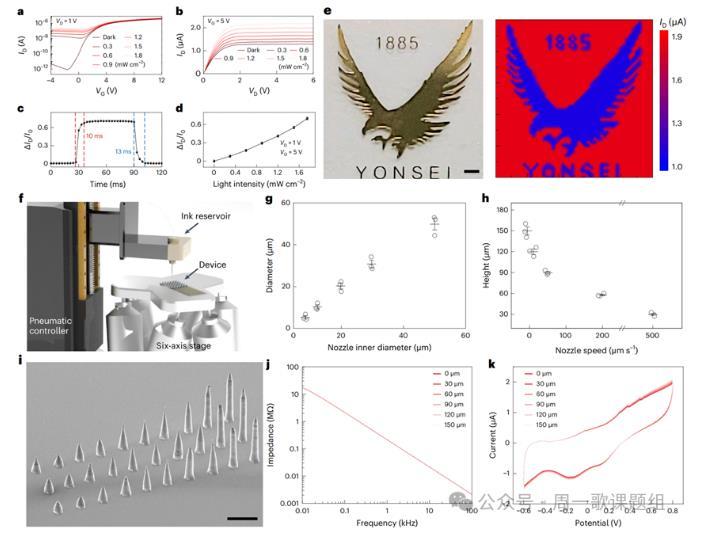
图2.光电晶体管阵列的光电特性和三维LM微电极的电化学特性。
然后,作者表征了该软性人工视网膜的光电及电化学特性。不同光强度照射下该设备显示出典型的光敏场效应晶体管行为(图2a-2b),并且具有较快的光响应和恢复时间(图2c)。此外,该晶体管阵列与入射光强度呈现线性比例(图2d)并且允许在光照期间观察通过鹰形荫罩图案的光(图2e)。为了得到一个柱状3D LM微电极阵列作为刺激电极,作者使用具有高分辨率打印的3D直接打印系统(图2f)。其中玻璃毛细管嘴的内径决定了EGaln柱的直径,载物台的纵向下降速度决定支柱的高度(图2g-2i)。此外,循环伏安曲线表明了该器件的阻抗和电荷存储容量不随支柱的高度而显著变化(图2j-2k)。
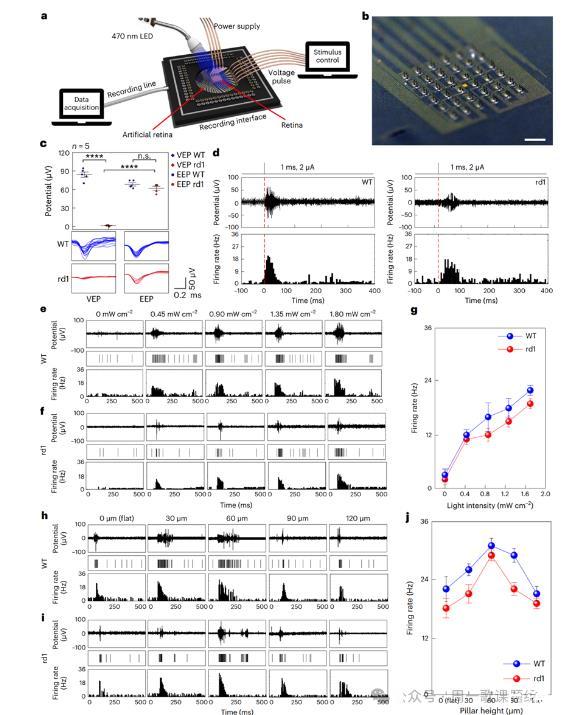
图3.使用WT和rd1小鼠视网膜的离体实验。
随后,作者使用野生型(WT)和rd1小鼠的视网膜探究了该器件的体外电生理作用,包括光、电刺激和电极的影响。先是记录了它们的视网膜在3D LM微电极上通过视觉或者电诱发时的反应,每个记录电极与每个刺激电极相邻放置(图3a-3b)。将来自WT和rd1小鼠的分离的视网膜放置在该设备上,3D LM微电极朝向视网膜的RGC侧。通过在没有设备操作的光照下记录了它们的视觉诱发电位(VEPs),而电诱发电位(EEPs)在黑暗状态下利用设备操作时进行记录。此外,由于小鼠是只有两种视锥细胞类型的两色哺乳动物(对蓝光和绿光敏感),因此视觉诱发使用470 nm的蓝光。结果显示光线没有在rd1小鼠视网膜内引起视网膜反应(图3c)。而在电诱发实验中,两种小鼠的视网膜均出现可比EEP量级的RGC尖峰,而且rd1小鼠比WT型放电活动更早、增强更明显(图3d)。已知rd1小鼠视网膜的形态学变化,包括RGC大小和内核层厚度的减少,会影响RGCs的功能特性,导致刺激阈值增加和潜伏期延长。接着作者分别使用平面型电极和具有不同高度的3D LM微电极在不同强度的光照下对两种视网膜进行设备操作时诱发EEP(图3e-3i),结果显示在平面型电极上诱发的RGC荆波放电率和光强度成比例增加(图3g)。与rd1情况相比,由于正常感光层的天然反应,WT小鼠视网膜显示出更高的放电率。而尽管柱状微电极具有与高度无关的电化学特征,但柱状结构电极在电刺激过程中增加了RGCs的放电活动(图3j)。且当高度超过90μm时射速再次下降。这可能是由于刺激尖端穿过目标RGCs时误将RGCs作为目标造成的。
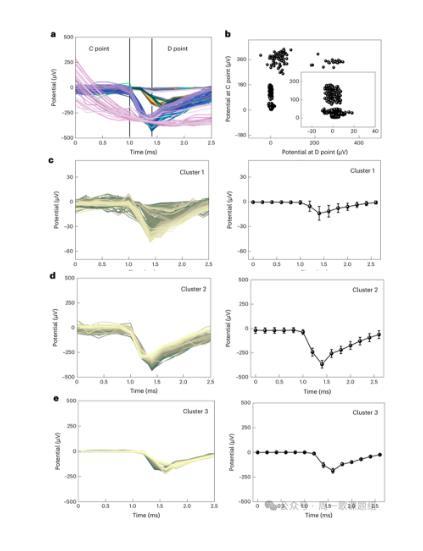
图4.用无监督机器学习的信号分类。
考虑到视网膜活动的复杂性,作者利用无监督机器学习进行信号处理。根据信号的大小和形状,给定的数据被分为不同的组(图4a)。然后,进行了K-均值聚类,将初步分类的信号作为输入数据。结果显示视网膜尖峰数据被进一步分类为具有不同潜在价值大小的四个聚类(图4b)。通过无监督的机器学习来分析这些分类的视网膜尖峰,以获得具有标准偏差的平均信号。此外,聚类1、2和3的同一聚类内的信号显示了相似的潜在值形式和时间持续时间(图4c-e)。当刺激RGC体细胞时,典型的细胞外记录的尖峰反应显示膜电位迅速降低(去极化),随后增加(复极),而RGC轴突显示相反的尖峰反应。3D LM微电极电刺激后立即记录的分类RGC信号波形仅呈现亚毫秒去极化的躯体RGC反应。这些结果表明了使用3D LM微电极选择性刺激RGC体细胞的潜力。尽管轴突刺激无法消除,但这种对RGC体的选择性刺激有可能减少轴突激活,从而导致更自然的视觉和更少的不规则感知。
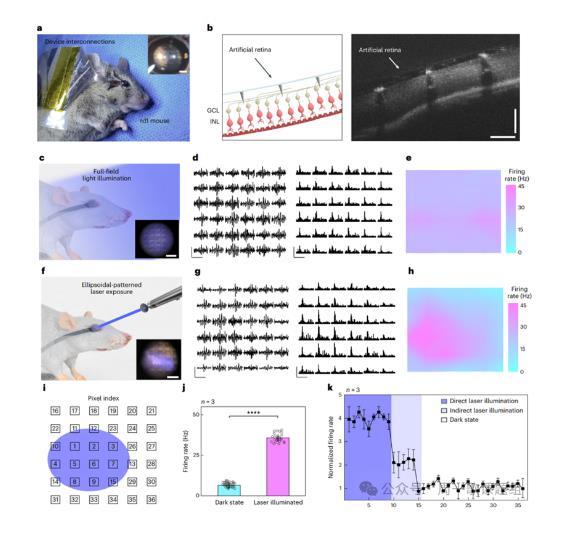
图5.使用活rd1小鼠进行视力恢复的体内实验。
最后,作者将具有3D LM微电极的人造视网膜装置植入体内活的rd1小鼠(n=3)中,确认感光层完全简并后进行活体小鼠的体内视力恢复实验。适配后的结果显示该装置很好地附着在视网膜表面,没有明显的损伤或出血(图5a)。而且,手术后获得的横截面光学相干断层扫描图像表明,3D LM微电极被视网膜组织共形包围,而没有塌陷(图5b)。作者通过恒定光照下诱发尖峰的电位和发射速率的实时迹线以及在该光照期间对发射速率进行了空间映射。通过与无光照明的情况相比证明了该设备在受刺激的视网膜区域具有良好的均匀性(图5c-5e)。此外,作者还使用激光通过椭球形图案的阴影掩膜选择性地暴露局部区域以验证退行性视网膜反应,结果显示光照区域表现出相对较大的视网膜响应(图5f-5g)。值得注意的是,当RGC轴突受到电刺激时,电刺激会发生逆向传播,导致黑暗状态下的错误RGC反应。最大发射率(即感受野)的空间分布与这种照明的椭圆形非常相似(图5h)。而且分类RGC尖峰显示了与离体结果相似的体细胞RGC反应的典型波形。为了定量比较激光照射和激光非照射区域(即黑暗状态)的视网膜反应,每个记录电极(像素)的位置被标记为索引(图5i)。然后,对全亮像素(指数1-9)和暗态像素(指数16-36)记录的最大发射率进行平均。完全暴露区域的RGC放射性比本底RGC放射性大约高四倍,充分证明了该器件在体内应用的潜力。
总结
作者报道了一种柔性人造视网膜,具有直接打印的3D LM微电极,能够进行微创视网膜刺激。体内实验表明,可见光照明诱导了光线入射的局部视网膜区域的RGCs的尖峰活动,表明活rd1小鼠具有视力恢复的潜力。这些结果对不均匀视网膜变性患者的个性化人工视网膜的开发具有预后意义。
作者还探究了设备尺寸的进一步扩大和像素数量的增加使其能够应用于具有更大眼球和更厚视网膜的大型动物模型。减小刺激电极尺寸对于实现高分辨率刺激至关重要。作者认为,对纳米级材料(例如,Pt纳米团簇)的进一步研究,通过在电极表面增加纳米级粗糙度来增强刺激效果,可能是一项在未来实现更有效视力恢复的具有重要潜力的工作。