热线:021-66110810,66110819
手机:13564362870


热线:021-66110810,66110819
手机:13564362870
在世界范围内,不同人类种群之间会在体质、形态等方面存在差异;但绝大多数 人肠道微生物组 (肠道菌群)中却有着许多相同的细菌和古细菌物种。众所周知,这些小生命与人类健康密切相关,并已被广泛的研究证实,它们是导致人类各种疾病的“始作俑者”,并且大多数仅活在人类肠道中。
生活在不同国家或地区的个体,肠道细菌组成和多样化会存在明显的差异。虽然,饮食是其中一个重要的决定因素,但这种特异性是否来自人类与其微生物之间共同进化的历史有关?到目前为止,关于人类肠道中的细菌来自哪里还是一个悬而未决的问题。2022年9月15日,发表在《 Science 》上的一项新研究中,来自马克斯普朗克生物学研究所微生物组科学系领导的研究团队在非洲、亚洲和欧洲的个体微生物组数据中首次系统比较了人类与其肠道细菌的进化史,发现了两者共同进化的证据。

先前的研究表明,肠道细菌谱系的一小部分与原始人类祖先一起形成了物种,但这种共同多样化模式是否在人类宿主中扩展还有待证实。自从人类走出非洲后,人口在全球范围内不断增长。饮食和生活方式也随着时间推移发生了巨大的变化。然而,特定的肠道细菌菌种不但没有消失,而且已经与人类“同呼吸,共命运”。因此,识别与人类共存的菌种对于理解肠道细菌如何随着其人类宿主的共同进化,以及两者之间的相互作用具有重要意义。 在这项新研究中,该团队首次系统地比较了人类与其肠道微生物的进化史。他们为来自加蓬、越南和德国的1225名母子参与者(839名母亲和386名儿童)及其肠道中发现的59个微生物分类群创建了系统发育树,以评估人类种群之间和种群内共享的肠道细菌菌种之间的共同多样化,并使用统计测试来调查这些发育树的匹配程度。
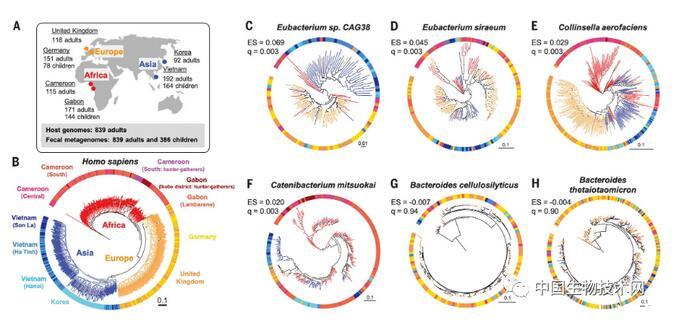
他们发现, 36个(61%)分类群与其人类宿主的进化历史相匹配。这意味着,当第一批人类走出非洲后的大约10万年间,这些肠道细菌就与其宿主“形影不离”,二者“携手”共同多样化(共同进化)。在国家与国家之间,和国家内部,人类及其肠道细菌的平行进化历史都是显而易见的 。
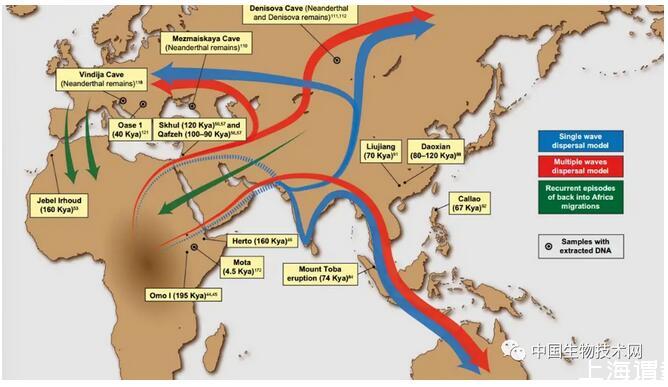
研究人员表示,对肠道细菌会如此密切跟随其人类宿主进化历史这一事实感到惊讶。同样值得注意的是,与人类历史最密切相关的菌种是那些现在最依赖肠道环境的菌株 。事实上,一些与人类一起进化的细菌(如 厚壁菌门 )在很大程度上依赖于人类肠道环境,它们具有更小的基因组,并且对氧气水平和温度更加敏感。这些特性使它们难以在人体外生存。相比之下,与人类历史关联较弱的细菌(如 拟杆菌属 )表现出更多与自由活细菌相似的特性。
一些肠道细菌的行为就像它们是人类基因组的一部分,正处在从“自由的活细菌’到依赖人体环境的梯度上,它们显示出似乎已经获得了对宿主不可逆的依赖性。这从根本上改变了我们对人类肠道菌群的看法。 随后,研究人员对儿童参与者(平均年龄7.4个月)的肠道宏基因组进行了采样。与其母亲的数据结合分析,让他们有了一个前所未有的机会来测试儿童肠道菌群的共同多样化模式。在测试的20个最常见的儿童分类群中,有9个显示出共同多样化的证据。其中, 长双歧杆菌显示出最有力的共同多样化 。几个分类群的协同多样化信号在加蓬和德国的儿童中得到扩展,但在越南儿童参与者中没有被发现。这些结果表明 ,生命早期肠道常见的细菌也与人类共同多样化。
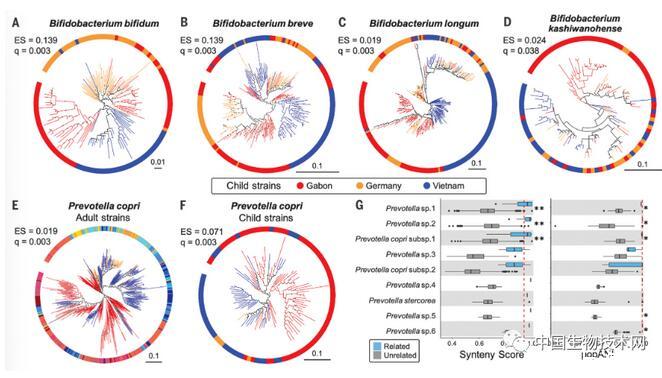
此外,研究人员还通过分析来自喀麦隆、韩国和英国参与者的类似数据集发现了同样的结果。该团队表示,与肠道菌群相关的人类健康状况从营养过剩、过敏、再到一系列重大慢性疾病。这些疾病的发病率与人种群有关,而肠道菌群的多样性也与人种群有关。已知一些与人类共存的菌种,如 普雷沃氏菌 (Prevotella copri), 直肠真杆菌 (Eubacterium rectale)和 长双歧杆菌 (Bifidobacterium. longum),它们的功能会根据人类种群的不同而存在差异。因此, 对不同人群肠道细菌菌株差异的认识将带来靶向微生物组的个性化疗法 。总之,这项研究结果强调了针对特定人群开发靶向微生物组疗法的重要性。