热线:021-66110810,66110819
手机:13564362870


热线:021-66110810,66110819
手机:13564362870
结果
牙菌斑介导有氧反硝化作用
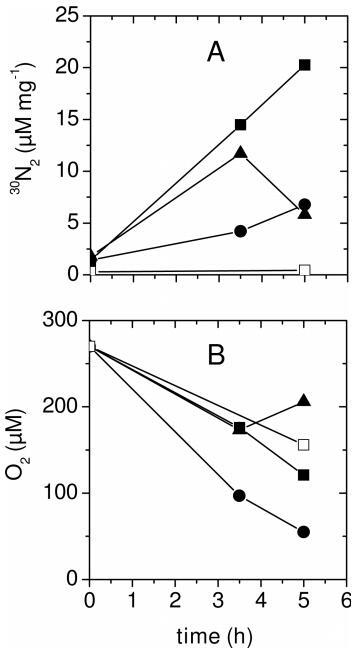
图1、牙菌斑中的反硝化作用。将三个人的牙菌斑悬浮在含有2%蔗糖和50μM Na15NO3的pH值为7.2的有氧矿物缓冲培养基中。在时间序列实验中测量了(a)30N2(单位:μM/mg蛋白质)和(b)表观O2浓度(单位:μM)的形成。每个符号类型代表一个人牙菌斑培养的30N2和O2测量值。对照组是在没有Na15NO3的情况下进行的。
牙菌斑通过反硝化作用将NO3-转化为N2。在培养分散的牙菌斑过程中,15NO3-生成30N2就证明了这一点(图1a)。
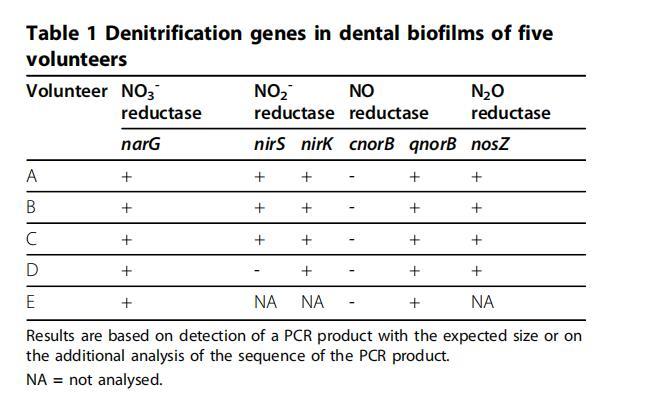
表1、五名志愿者牙齿生物膜中的反硝化基因。
通过聚合酶链式反应(PCR)检测将NO3-还原成N2所需的所有基因(NO3-还原酶、NO2-还原酶、NO还原酶、N2O还原酶),证实了牙科生物膜中存在完全的反硝化作用(表1)。呼吸作用NO还原酶的基因仅限于存在依赖喹啉型(qnorB),而不存在依赖细胞色素c型(cnorB)。
有两个证据表明,牙科生物膜中的反硝化作用是在有氧条件下发生的。首先,我们观察到悬浮在添加了50μM 15NO3-的空气饱和培养基中的牙菌斑产生了30N2(图1a)。该培养基中的氧气测量结果表明,有氧异养呼吸不会导致培养期间出现缺氧情况(图1b)。
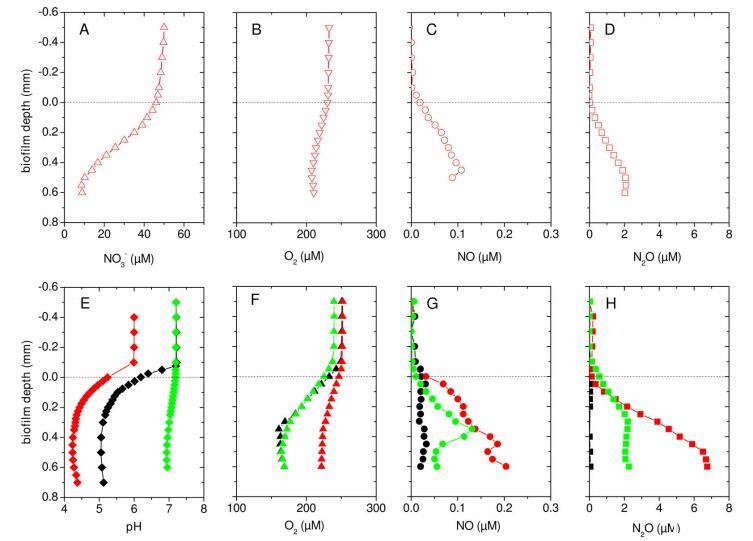
图2、原位检测口腔外牙科生物膜的代谢活动和微环境条件。微电极测量牙菌斑中NO3-、O2、NO、N2O和pH的浓度曲线。培养基中含有非缓冲矿物混合物和2%的蔗糖。a-d显示的是上层培养基中50μM NaNO3(红色)的测量结果。e-h显示了在无NaNO3(黑色)和有760μM NaNO3(红色和绿色)时的测量结果。绿色符号显示的是在磷酸盐缓冲盐水(pH7.2)和760μM NaNO3存在的情况下进行的测量。水平线代表生物膜表面。测量是在同一样本点进行的,因此具有直接可比性。
其次,微电极测量显示,在有O2存在的情况下,NO3-被消耗,并且在有O2存在的情况下,还形成了反硝化中间产物NO和N2O(图2a-d)。在如此低的NO3-浓度下,可以想象所有的NO3-都被用于同化成生物质,因此无法用于呼吸脱氮。然而,在该斑块样本中,当NO3-浓度为50μM时,NO3-并未被完全消耗(即NO3-并非限制性的)(图2a)。因此,在50μMNO3-浓度下,NO3-同化和反硝化作用肯定已经达到最大能力。将NO3-浓度进一步提高到760μM很可能不会改变这两种途径对NO3-总吸收量的贡献。反过来,生物膜在760μM的NO3-浓度下仍保持缺氧状态,并产生反硝化中间产物NO和N2O(图2f-h),这表明在高浓度NO3-下,有氧反硝化也很活跃。
斑块脱硝过程中化学和生物NO和N2O的形成与pH值有关
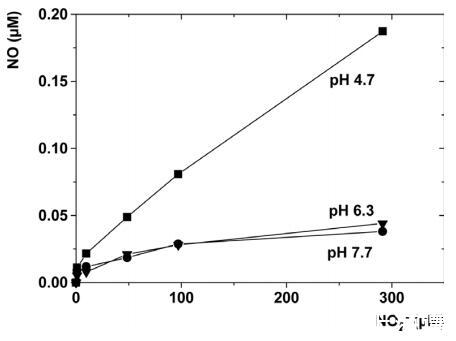
图3、通过酸性分解NO2-形成NO。在不同pH值的磷酸盐缓冲盐溶液中滴定不断增加的NO2-浓度时,使用NO微电极测量NO的形成。
NO3-是牙科生物膜中NO和N2O的来源。NO和N2O的形成仅限于NO3-的存在(图2g,h)。牙科生物膜中NO的形成是由生物NO2-还原和NO2-的酸性分解介导的。在非缓冲培养基中,细菌活性降低,生物膜pH<5(图2e),深度平均NO浓度从0.08μM增加到0.15μM(图2g)。在pH值为4.7的缓冲液中滴定50μM的NO2-,结果表明NO2-的酸性分解会导致约0.05μM NO的化学形成(图3),这与在pH值小于5的生物膜中观察到的增加处于同一范围。NO2-也能在唾液中自然积累到50μM或更高的浓度。综上所述,这表明在牙菌斑pH值较低时,NO2-的酸性分解有助于NO的形成,而生物NO的形成仍可能同时发生。
从反硝化代谢平衡的角度来看,酸性条件导致的NO绝对增加量很小。这一点很明显,因为在酸性条件下,N2O(NO的还原产物)的深度平均增加量比NO浓度的增加量高出约两个数量级。这表明生物膜细菌能有效地将大部分NO转化为N2O,从而将细胞毒性NO的稳态浓度保持在较低水平,这在环境生物膜中也有观察到。
NO的形成会减少牙菌斑对O2的吸收
在中性pH下,NO3-存在下的氧气吸收量高于酸性条件下的氧气吸收量(图2e、f)。O2曲线显示,O2通量减少了50%,即从缓冲条件下的-105nmol/cm2/h降至非缓冲条件下的-43nmol/cm2/h。在没有NO3-的情况下,仅酸性pH值不会导致氧气吸收量减少,因为氧气通量为-143nmol/cm2/h。细菌O2消耗量的减少可能是由于最高NO浓度(0.15至0.2μM)的直接毒性作用造成的,如NO与末端呼吸性O2还原酶的结合。然而,从0.08μM到0.2μM的绝对浓度增加可能不会影响呼吸作用,因为以前的研究表明,0.8μM以上的浓度是抑制大肠杆菌中O2还原所必需的。此外,一小部分电子不仅不会促进O2的还原,反而可能被优先用于通过还原成N2O来解毒NO,从而导致N2O浓度升高和O2吸收受到抑制(图2f,h)。
人类口腔中N2O的产生取决于唾液中的NO3-和牙菌斑的存在
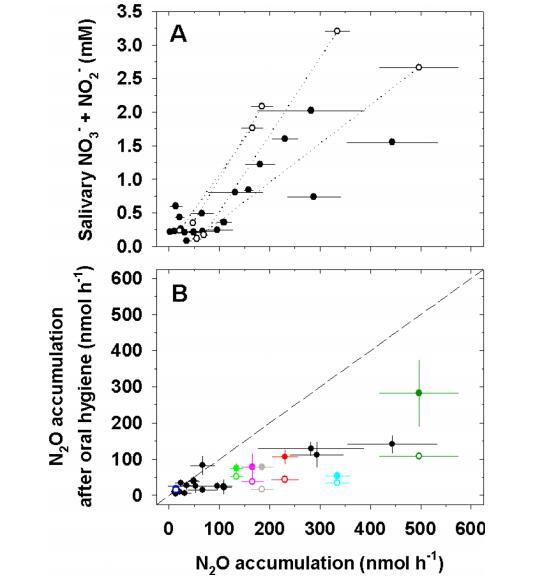
图4、(a)15名未刷牙志愿者的口腔N2O生成量与唾液中NO2-/NO3-浓度的相关性。每个数据点代表一个人在某一天的口腔N2O累积率(黑点)。有些志愿者不止一天被采样,因此总共有19个数据点。四名志愿者在饮用富含NO3的甜菜根汁前后进行了额外采样,以增加唾液中NO2-/NO3-的浓度和口腔N2O的积累(虚线连接的白圈)。(b)口腔卫生对口腔N2O积累率的影响。刷牙前个人的口腔N2O积累率与刷牙后的N2O积累率对比图(黑点)。六个人在刷牙后使用了可影响整个口腔细菌的杀菌漱口水(圆圈,六个人各用一种颜色表示)。例如,一个人(深绿色)的口腔一氧化二氮累积率为500nmol/h,刷牙后,其累积率降至290nmol/h。随后使用漱口水的结果是110nmol/h。虚线表示口腔卫生对口腔N2O积累没有影响。误差条表示五次重复测量口腔N2O积累率的标准误差。
我们培养了人类口腔中的空气("口腔空气"),并测量了N2O的积累率,以量化口腔生境中脱氮的活体意义。将口腔空气中的N2O积累与牙齿生物膜的存在和唾液中的NO3-/NO2--浓度联系起来(图4)。在有牙菌斑的情况下,不同受试者的N2O积累量差异很大,从11到443nmol/h。不同受试者的N2O积累量随着唾液中NO3-/NO2-浓度的增加而增加(图4a)。饮用200毫升含有12毫摩尔/升NO3-的甜菜根汁会增加唾液中NO3-/NO2-的浓度,从而导致口腔N2O积累速度增加3.8到9.1倍。
牙齿生物膜是人类口腔中产生N2O的主要场所。这一点很明显,因为在普通刷牙的同时使用杀菌漱口水可使口腔N2O的累积率降低82%,而单独刷牙可使口腔N2O的累积率降低62%(图4b)。