热线:021-56056830,66110819
手机:13564362870


热线:021-56056830,66110819
手机:13564362870
植入式生物电子学为实时和连续监测活体生理信号提供了前所未有的机会。大多数生物电子学采用薄膜衬底,如聚酰亚胺和聚二甲基硅氧烷,表现出高水平的柔性和可拉伸性。然而,这些薄膜的低透气性和相对高的模量阻碍了长期的生物相容性。相比之下,在多孔基底上制造的器件具有高透气性的优点,但图案密度低。
创新点
香港理工大学Zijian Zheng和香港城市大学Xinge Yu课题组提出了一种晶圆尺度的高分辨率制造策略,用于超软,可拉伸和高透气性的液态金属微电极(μLMEs)。通过光刻技术在4英寸弹性纤维毡上展示了2μm的图案化能力,或高达~75,500个电极/cm2的超高密度μLME阵列。植入μLME阵列作为神经接口,对活体大鼠的皮质电图信号进行高时空定位和干预。植入的μLMEs具有8个月以上的长期生物相容性。
文章解析
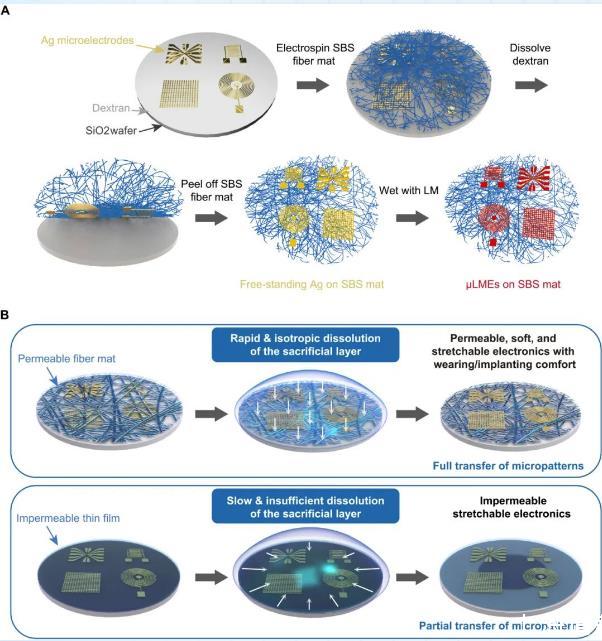
图1:可拉伸和可渗透的液态金属微电极(μLMEs)的制备过程。(A)μLMES制造过程的示意图。(B)比较使用可渗透的纤维垫或不可渗透的薄膜对牺牲层的不同溶解过程影响示意图。
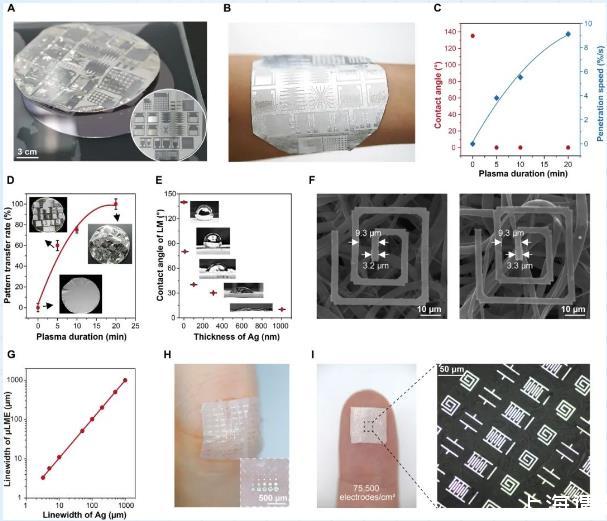
图2:μLMEs结构示意图。(A)银微图案从晶圆转移到SBS纤维垫的图像。插图为转移之前在晶圆上的图案。(B)附着在人体手臂上的μLMEs的图像(液态金属负载量:10 mg/cm2)。(C)溶剂对牺牲层的接触角和渗透速度以及(D)图案转移成功率与等离子体处理时间的函数。(E)LM在转移银层上的接触角随银厚度的变化。(F)选择性润湿前后SBS纤维垫上电极的扫描电镜图像。(G)μLMEs的线宽与Ag电极的原始线宽的对应关系。(H,I)μLMEs高密度阵列的,阵列密度高达75500电极/cm2。
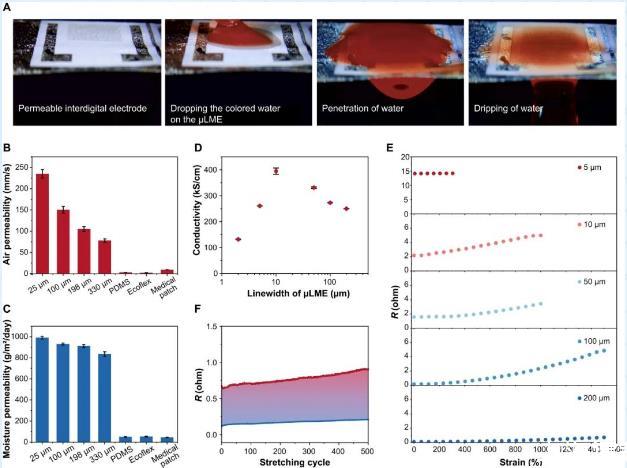
图3:μLMEs的渗透性、导电性和拉伸性表征。(A)一个彩色水滴从μLMEs的一侧渗透到另一侧光学图像。(B,C)μLMEs在不同厚度SBS纤维垫上以及其他生物电子学常用衬底,包括PDMS,Ecoflex和医疗贴片上的透气性和透湿性表征。(D)不同线宽下μLMEs的电导率变化。(E)不同线宽μLMEs在不同拉伸应变下的电阻。(F)在1000%的大拉伸应变下μLMEs(线宽50μm)的循环电稳定性。
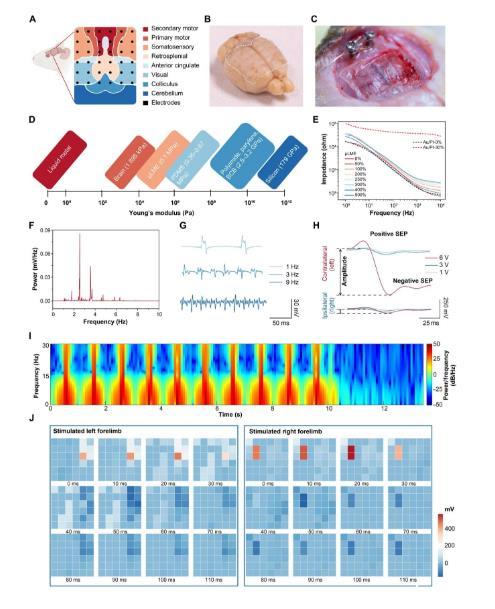
图4:基于高密度μLMEs的神经电生理界面生物电子学表征。(A)基于μLMEs的ECoG阵列的示意图和记录的皮质子域。(B,C)μLME ECoG电极阵列(厚度25μm)在柔软、弯曲和复杂的大脑皮层上适形附着的数字图像。虚线表示μLME阵列的边界。(D)μLMEs的杨氏模量与已经报道的ECoG生物电极材料的比较。(E)不同应变下μLMEs和Au/PI电极的体外电化学阻抗谱(EIS)表征。(F)活体大鼠睡眠状态下体内神经信号的功率谱分析。(G)用μLMEs记录不同频率脉冲电压电刺激下的体感诱发电位(SEPs)。(H)不同强度脉冲电压电刺激下对侧和同侧体感觉皮质电位的比较。(I)对侧体感觉皮层在10次强度为6 V、频率为1 Hz的连续电刺激下的信号谱图。(J)左右前肢电刺激下μLME阵列的时空特性研究。
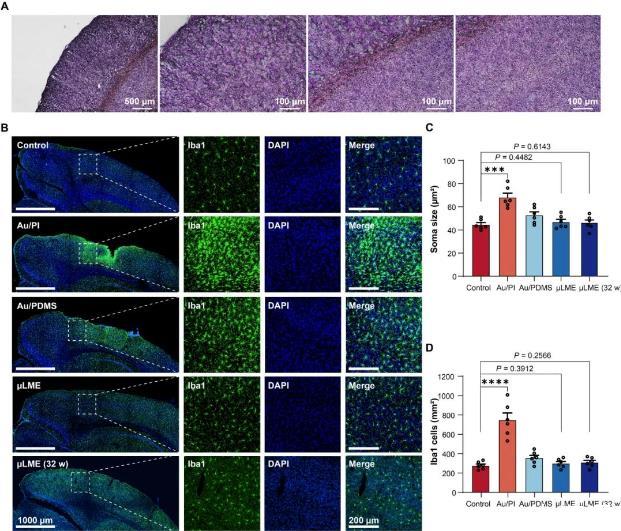
图5:μLMEs用于慢性神经植入物的慢性(长期)生物相容性表征。(A)电极阵列植入2小时后染色脑切片的免疫组织学分析。(B)对照植入后2周,Au/PI电极、Au/PDMS电极、μLME电极和μLME电极,植入时间为32周(32w),免疫组化染色小胶质细胞(Iba1,绿色)和细胞核[4′,6-二氨基-2-苯基吲哚(DAPI),蓝色]。左图为低放大图(比例尺=1000μm),右图为高放大图(比例尺=200μm)。(C)小胶质细胞胞体大小的统计分析(n=6)。Au/PI组(P=0.0002)和Au/PDMS组(P=0.0375)的小胶质细胞胞体大小与对照组相比显著增加(双向,非配对Student's t检验)。μLME组与对照组之间差异无统计学意义(植入后2周P=0.4482,植入后32周P=0.6143)。(D)总小胶质细胞数量的统计分析(n=6)。与对照组(双向,未配对的学生t检验)相比,在AU/PI组(P<0.0001)和AU/PDMS组(P=0.0274)中发现了IBA1细胞的显着增加。μLME组和对照组之间没有发现显着差异(植入后2周时P=0.3912,在植入后32周时P=0.2566)。
结论与展望
作者提出一种晶圆级高分辨液态金属微电极(μLME)的制备方案,在超软,可拉伸和高透气性纤维垫上实现了每平方厘米75000个电极的图案分辨率,这些μLME显示出优异的机械柔性,当延伸至1000%应变时仍表现出出色导电性,以及在皮肤附着和植入测试中的生物相容性,并且可以用于脑皮层电信号的采集。这一方案为高密度,可集成,可植入的生物电子提供了解决思路。
 相关新闻
相关新闻